ニュースの要点
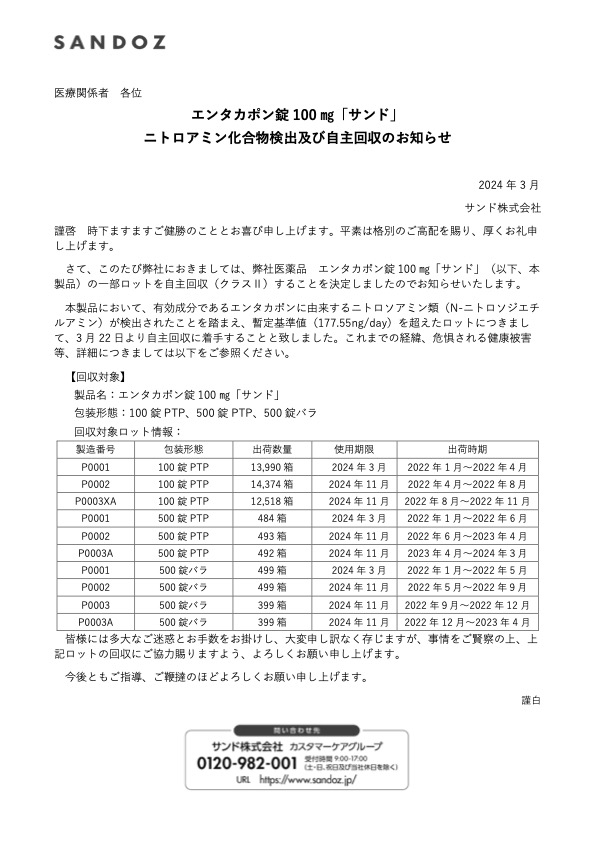
サンド株式会社は3月22日、エンタカポン錠 100 ㎎「サンド」の一部ロットにおいて、有効成分であるエンタカポンに由来するニトロソアミン類(N-ニトロソジエチルアミン)が検出されたことを踏まえ、暫定基準値(177.55ng/day)を超えたロットについて、3月22日より自主回収(クラスⅡ)すると公表した。
エンタカポンは,原薬中にジエチルアミンが存在するリスクがあり,ジエチルアミンは,亜硝酸塩により N-ニトロソ化されやすくNDEAを形成する可能性がある。
NDEA は既知のニトロソアミン類であり、許容摂取量は 26.5 ng/日(エンタカポンの1日最大用量を1600mgとした場合:0.0165ppm)とされている。しかし、エンタカポンの累積治療期間は、比較的短い期間投与された後、トリプルコンビネーション製品を使用するのに便利なスタレボ治療に切り替えられるため、1年未満であると考えられている。従って、ICH M7に示される一生涯よりも短い期間(LTL:less-than-lifetime)のアプローチに基づき、最も保守的な調整係数(6.7×許容摂取量)を用いて算出した 177.55 ng/day(6.7×26.5 ng/day)を管理値として設定した。
本製品は国内における販売期間から、約2年3か月が最長の投与期間であり、現時点において患者様への重篤な健康被害のおそれはないと考えているとしている。
※ニトロソアミン類は、長期間にわたって許容範囲を超えて摂取した場合、発がんのリスクを高める可能性があることから、本邦では 2021年10月に厚生労働省から「医薬品におけるニトロソアミン類の混入リスクに関する自主点検について」が発出され、自主点検の実施が指示されていた。

(https://www.neurology-jp.org/news/pdf/news_20240321_01_01.pdf)